
新闻动态
硅酸铝镁在制剂领域研究与应用的进展
来源:未知 | 作者:admin | 发布时间: 2018-03-18 21:52 | 次浏览
| 分享到:
硅酸铝镁在制剂领域研究与应用的进展
一个喜欢酒后吹牛的药剂学工作者的综述
吹牛(二)
硅酸铝镁(NEUSILIN®)是一种非晶态无定型粉末,包含铝的四面体或八面体,镁的八面体和硅的四面体,几者随机连接形成一个复杂的三维结构,而不是由单一明确的单体结构重复排列而成。自上世纪60年代由日本富士化学公司将硅酸铝镁开发作为药用辅料上市至今,已有近60年的历史。由于其特殊的分子结构及立体构型,使其具有良好的流动性、可压性、吸附性、粘合性、粉体性、填充性以及助悬性等特点,从而使其在药物制剂的应用领域发挥了卓越的作用。随着现代药剂学的研究进展,近期,又不断发现了一些硅酸镁铝在制剂设计方面的新用途,为其展示出更为广阔的应用前景。
一.化学结构与一般性质
化学结构式及电镜照片如图1所示:
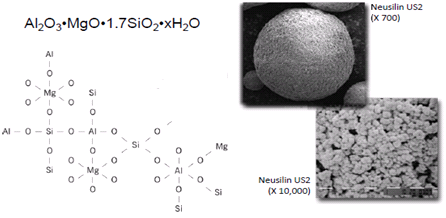
图1.化学结构式及电镜照片
CAS号:1327-43-1
性状:白色,无嗅粉末。几乎不溶于水和乙醇,可溶于热的稀盐酸。
pH值:(4%水浆)6.0-8.0。
干燥失重:小于20%。
酸消耗量:按干燥品计算,每克硅酸铝镁消耗0.1mol/L的盐酸不低于210ml。
二.安全性
急性毒性:按照600-6000mg/kg的剂量标准给雌性小鼠灌胃,连续14天。在6000mg/kg剂量组中,观察到小鼠体重呈下降趋势,自发运动减少,但是,停止灌胃后第10天,上述症状得到恢复。
亚急性毒性:Ueno等人与1978年做了一项关于硅酸铝镁的毒性实验,按照1500mg/kg剂量与甘草提取物一起给Wister immichi大鼠灌胃,连续给药30天,没有显示任何毒性反应。在体重、食物与水的消耗量、血液学、生化以及鸟检测,对照组与实验组没有显著性差别。尸检和组织学检查也未见明显病变,证明了硅酸铝镁的安全性良好。
最大用量:硅酸铝镁(NEUSILIN®)是一种安全性较高的辅料,根据日本医药添加剂百科全书(Encyclopedia of the pharmaceutical additives, Japan, 2005)规定,每日口服最大用量为1.05g。
三. 硅酸铝镁(NEUSILIN®)的型号与特性
硅酸铝镁(NEUSILIN®)共有11种型号,表1列出了4种常用型号的物理性能,见表1所示。型号的区分取决于pH值(水浆液)、粉末或颗粒以及水分含量等。表2介绍了两种型号硅酸铝镁对难闻性气味的吸附能力。
表1.硅酸铝镁的型号与各项性能指标对比
*二次团聚粒径(Secondary agglomeration particle size)
表2.硅酸铝镁((NEUSILIN®NFL2)对难闻性气味的吸附能力
四.硅酸铝镁在药剂学中的应用
从生物药剂学的观点出发,通常认为药物从固体剂型中的溶出依赖于溶解性,药物的吸收则依赖于渗透性。固体剂型的设计能否达到的生物药剂学及物理药剂学要求,取决于所用辅料及其制剂工艺。硅酸铝镁的物理特性赋予其在药物制剂处方设计的独特功能,试归纳其特点如下:
1. 直接可压和助压缩性,提高片剂的硬度、粉体的流动性、防静电以及防止粉体结块。
2. 具有高容量油脂吸附作用,使油状药物固体化。
3. 可提高易潮解药物吸湿稳定性。
4. 便于亲水性低熔点原料药物的压片。
5. 提高制剂处方的稳定性。
6. 缓控释处方的组成。
7. 通过球磨或固体分散技术,提高生物利用度等。
8. 提高固体制剂的外观质量。
表3.不同型号硅酸铝镁(NEUSILIN®)的用途应用和用量
表3为不同型号硅酸铝镁(NEUSILIN®)作为制剂添加剂不同用途及常规用量。前面介绍了硅酸铝镁的一般性能,以下从五个方面介绍硅酸铝镁在药剂学中研究与应用的案例及部分研究结果。
(一)提高片剂的硬度、粉体的流动性、防静电以及防止粉体结块等
图2是不同硅酸盐对淀粉-乳糖片硬度的影响,由图可见,处方中添加10%的硅酸铝镁(NEUSILIN®US2)与10%硅酸钙片剂的硬度相当,而添加硅胶处方的片剂硬度最低。硅酸铝镁(NEUSILIN®)单独与乳糖配伍压片,其增加片剂硬度的作用也是显而易见的,见图3所示。
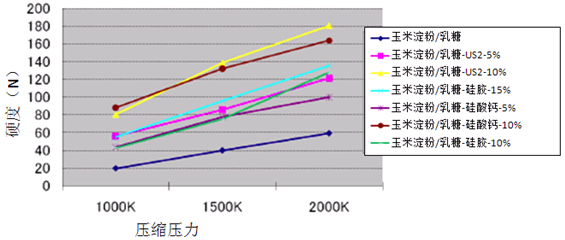
图2.玉米淀粉-乳糖-硅酸盐组方对片剂硬度的影响
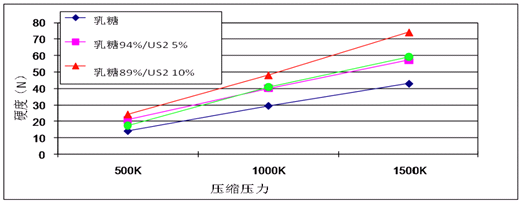
图3.硅酸铝镁(NEUSILIN®)对乳糖压片硬度的影响
图4为在马铃薯淀粉中加入不同浓度的硅酸盐后,粉体的休止角变化曲线。

图4.在马铃薯淀粉中加入硅酸盐的休止角曲线
图4为在马铃薯淀粉中加入不同浓度的硅酸盐后,粉体的休止角变化曲线。硅酸铝镁(NEUSILIN®)降低马铃薯淀粉的休止角用量最低。图5为硅酸铝镁(NEUSILIN®)与马铃薯淀粉混合后的电镜照片,硅酸铝镁(NEUSILIN®)是均匀粘附的于马铃薯淀粉颗粒的表面,就是这样起到增加流动性、防结块以及防静电作用的。

图5.硅酸铝镁与马铃薯淀粉混合后的电镜照片
在高湿条件下防止药物结块的典型例子是天冬氨酸钠,如图6所示。在天冬氨酸钠中加入5%的硅酸铝镁(NEUSILIN®),置RH75%环境下露置2天,仍能保持为松散的颗粒状,而不加硅酸铝镁(NEUSILIN®)者则明显结成了块状。

图6.硅酸铝镁的防天冬氨酸钠吸潮结块作用
表4是一组扑热息痛片剂处方,其中处方2、3、5含有2%的硅酸铝镁(NEUSILIN®UFL2),将试制的片剂于40℃,RH75%条件下放置1个月,所有加入硅酸铝镁(NEUSILIN®)片剂的硬度均无明显变化,而未加硅酸铝镁(NEUSILIN®)片的硬度则明显降低,溶出度未见明显变化,见图7所示。
表4.提高片剂硬度和溶出稳定性
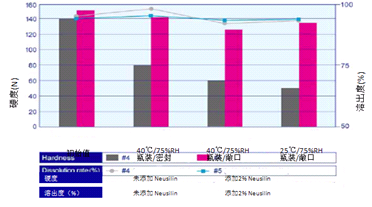
图7.硅酸铝镁(NEUSILIN®)对扑热息痛片硬度和溶出的影响
(二)油状药物的固体化或粉末化
有些药物属于油状液体,除了可以制成软胶囊外,有时也需要制成其他固体制剂或固体制剂添加剂,如脂溶性维生素类、DHA、挥发油等,有些难溶性药物还可用油脂类物质溶解,进而制成固体制剂,这都需要采用油状物质的固体化技术。硅酸铝镁(NEUSILIN®)的出现,为此类制剂的处方设计提供了有效的手段。从表1和图8可知,两种硅酸铝镁(Neusilin®US2和Neusilin®UFL2)的吸油能力达到3g/ml以上,可见其吸油能力之卓越。表5列出了以硅酸铝镁为吸附剂的亚麻油片的三种处方,由表5可见,添加有硅酸铝镁(Neusilin®US2)的处方,片剂硬度明显高于添加气相二氧化硅的处方。由图9可见,以硅酸铝镁(NEUSILIN®)为吸附剂,获得的亚麻油粉末经50℃干燥后,外观良好,明显优于气相二氧化硅和微粉硅胶作为吸附剂制成的产物外观。
表5.硅酸铝镁(NEUSILIN®)对亚麻油吸附片硬度的影响
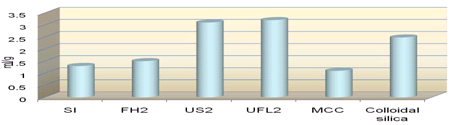
图8.不同硅酸盐吸附亚麻油的能力

图9.不同硅酸盐吸附亚麻油粉末化产物外观(50℃干燥后)
图10为维生素E与微晶纤维素混合压片张力强度与压缩压力的关系(左),图以及为维生素E与硅酸铝镁(NEUSILIN®)混和压片张力强度与压缩压力的关系(右)。
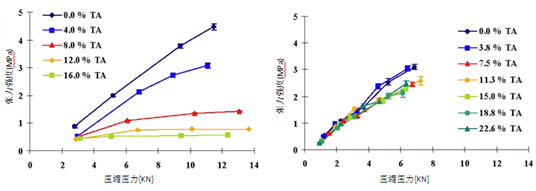
图10.维生素E与不同吸附剂混合压片后张力强度与压缩压力的关系
图11维生素E与微晶纤维素混合压片崩解时间与张力强度的关系(左),以及为维生素E与硅酸铝镁(NEUSILIN®)混和压片崩解时间与张力强度的关系(右)。
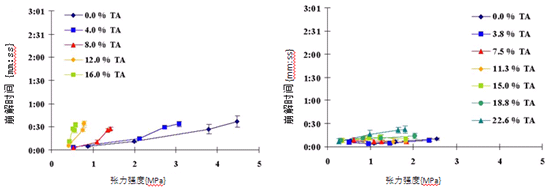
图11.维生素E与不同吸附剂混合后压片崩解时间与张力强度的关系
图12为维生素E片的溶出曲线,维生素E的溶出效果以硅酸铝镁(NEUSILIN®)为吸附剂压出的片剂优于以气相硅胶为吸附剂的片剂。图13是DHA片的处方以及两种处方片剂强度和溶出与压缩压力的关系。
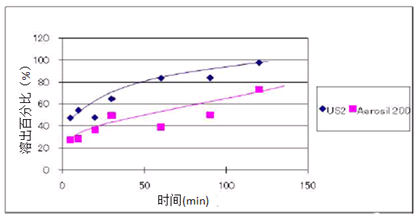
图12.维生素E片在pH1.2人工胃液中的溶出曲线
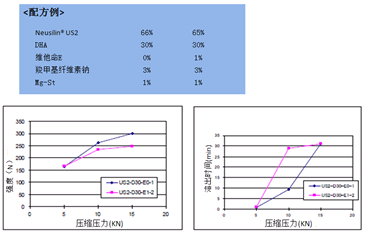
图13.硅酸铝镁(NEUSILIN®)吸附的鱼油片强度与压缩压力的关系
(三)固体药物通过与硅酸铝镁共研磨达到药物晶体的无定型化
选择合适的辅料与晶型难溶性药物药物进行研磨,可以药物晶形转变为无定型,并可防止再结晶、可提高润湿性、溶解度、溶出度乃至提高主药的生物利用度,硅酸铝镁(NEUSILIN®)就是这种研磨辅料的首选。因为硅酸铝镁含有多个硅醇基,通过与晶型药物共同研磨(或球磨),可与药物形成氢键结合,从而改善药物的物理性能。但这类研磨物不适合那些因晶型改变而稳定性下降的药物。对热敏感性药物可以考虑采用冷冻研磨方式。
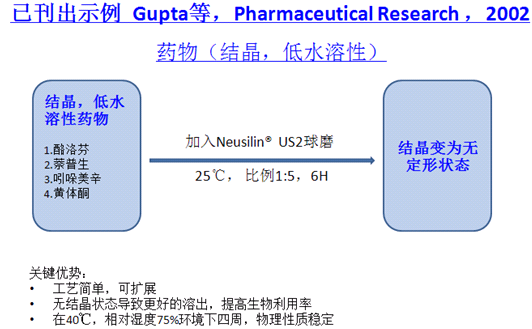
图14.研磨物制备示意图
Gupta等的研究报告表明,通过球磨的硅酸铝镁(NEUSILIN®)与一些药物如酮洛芬、吲哚美辛、萘普生和黄体酮等,可显著改善这些难溶性药物制剂的溶出度。其中与酮洛芬、吲哚美辛和萘普生在研磨过程中,酸性药物与硅酸铝镁产生酸碱反应,使主药形成无定型粉末,而黄体酮则是与中性硅酸铝产生了氢键结合,进而使主药形成无定型粉末。上述无定形粉末的X-射线衍射图谱中,主药晶体的衍射峰明显消失,经过加速试验稳定性考察(4周)证明,物理稳定性仍然良好。
醋氯芬酸与硅酸铝镁研磨物使醋氯芬酸的溶解性大幅提高。布洛芬与硅酸铝镁(NEUSILIN®)可形成溶解性更高的盐。

图15.吲哚美辛与US2研磨混合物的X-射线衍射图谱
(四)固体分散技术
此类制剂设计的主要目的是提高难溶性药物的溶出速度及生物利用度。图16是固体分散制剂组成示意图。
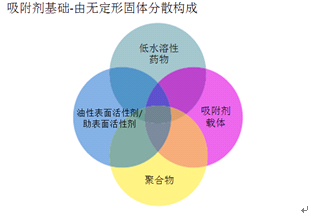
图16.无定形固体分散制剂组成示意图
不同的难溶性药物需要采用不同的固体分散物制备方法。图17是三种药物的固体分散体制备方法。图中标示的载体是指吸附剂,具有强大吸附能力的硅酸铝镁也许是最佳选择。图中的SMEDDS/SEDDS的含义是自乳化释药系统。
(1)熔融法:药物+聚合物以及表面活性剂共融,加载体(或不加)制成其他剂型。
(2)溶剂法:药物溶解+载体,加聚合物或与表面活性剂的混合物,脱除溶剂(或不脱),制成其他制剂。
(3)乳化法:药物溶于油,加表面活性剂或辅助表面活性剂,加载体,制成自乳化系统,进一步制成其他制剂。
上述三种固体分散技术均可使用硅酸铝镁(NEUSILIN®)作为载体。其次,关于表面活性剂的使用也不是绝对的,仅仅是在处方设计没有达到预期时才使用。用硅酸铝镁(NEUSILIN®)作为固体分散物载体具有载药量大、流动性好、可压性强、比表面积大、吸附能力好以及保护药物免受湿气影响的能力强等特点。

图17.三种固体分散物制备方式
图18是Gupta等发表的7种难溶性药物的固体分散物制备方法。图19和图20是难溶性丁酸类药物BAY-12-9556固体分散物和物理混合物的溶出曲线。

图18.七种难溶性药物的固体分散物制备方法
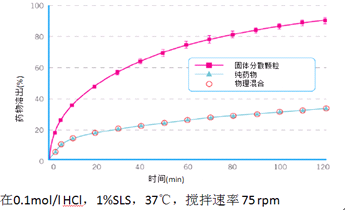
图19.难溶性药物BAY-12-9556固体分散物和物理混合物的溶出曲线

图20.不同配方的溶出曲线
图20中各条曲线的样品中主药成分BAY-12-9556与硅酸铝镁比例均为1:1,但硬脂酸聚乙二醇甘油酯的比例分别为0.5、1和1.5,随着硬脂酸聚乙二醇甘油酯比例的升高,溶出速度明显提高。
将难溶性药物二氢吡啶类药物用脂肪酸甘油酯类物质溶解,然后用硅酸铝镁(NEUSILIN®)吸附,再进一步制成固体制剂,也可获得较高的生物利用度的制剂。处方1和处方3的生物利用度分别为23%和29.4%,对照药(不加添加剂)仅为0.3%,而且在60℃连续加热4周,有关物质未见明显增加,稳定性良好。
表6.二氢吡啶衍生物的处方设计
2008年,Catarzi等发表了格列本脲自乳化固体分散释药系统的研究报告,他们选择了三种硅酸盐作为吸附剂,处方设计见表7。该报告还强调不能使用Aersil380、R972、200和Zeopharm177等作为吸附载体,因为会导致自乳化吸附后,流动性降低。图21为格列本脲自乳化制剂的的溶出曲线。
表7.格列本脲自乳化固体分散释药系统处方
*800ml自乳化配方:聚氧乙烯甘油癸酸酯(Labrafac-Hydro®)作为油相,吐温20作为表面活性剂,二乙二醇单乙基醚作为辅助表面活性剂。
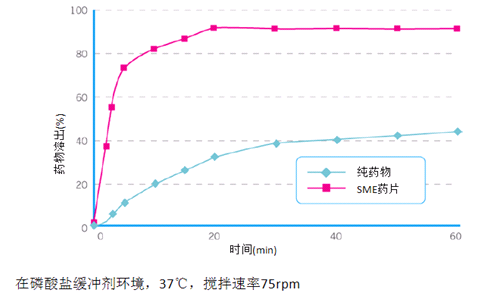
图21.格列本脲SMEDDS溶出曲线
Agarwal等人2009年用不同型号的硅酸铝镁Neusilin®和其他一些硅酸盐与灰黄霉素制备成自乳化释药系统,其中硅酸铝镁Neusilin® UFL2D自乳化制剂显示最高的溶出度(1小时>90%),并观察到其具有最大的吸附率,达到2.75ml/g,说明这种自乳化制剂的溶出度与吸附剂粒子的大小及其比表面积有明显的相关性。图22为这一系统的配方和制备过程及混合粉末的流变学数据。图23为采用不同载体作为吸附剂的溶出曲线,并与原料药粉末作对比。

图22.灰黄霉素自乳化制剂配方、制备过程及混合粉末的流变学数据

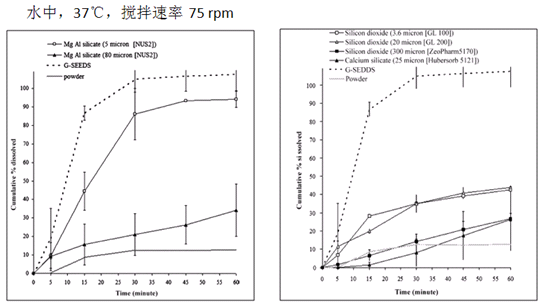
图23.灰黄霉素自乳化释药系统的溶出曲线
Suhas G. Gumaste等报道了不同硅酸盐吸附油脂和表面活性剂对压片性质和表面结构的影响,结果表明:6种硅酸盐按1:1比例吸附Capmul®MCM EP(甘油癸酸酯)、Captex®355 EP/ NF(辛酸/癸酸甘油三酯)和Cremophor®EL(PEG-35蓖麻油)后,加入20%的微晶纤维素后压片,测量片剂的抗张强度。硅酸铝镁Neusilin®®US2是唯一能够生产出具有可接受的抗张强度的片剂,表面结构研究发现脂质液体是被吸附到的硅酸盐孔隙中。
Mladen等报道了水难溶性药物卡马西平固体自微乳化药物递送系统(SSMEDDS),处方中选用的表面活性剂为吐温80和辅助表面活性剂PEG-40氢化蓖麻油和油辛酸/癸甘油三酯,表面活性剂与辅助表面活性剂的比率为1:1,分别采用4种硅酸盐作为吸附剂,为Neusilin®(®)UFL2、Neusilin®(®)FL2、SYLYSIA(®)320和SYLYSIA(®)350。研究发现(SSMEDDS)制剂可改变卡马西平的溶出速率,吸附剂的类型对卡马西平的溶出速率也有显著影响。
另有文献报道了采用硅酸铝镁(NEUSILIN®)为吸附剂,将扎来普隆、优降糖、盐酸乐卡地平、环抱素A以及帕潘立酮等难溶性药物制成纳米自乳化粉末或片剂,均使主药的溶解性和溶出度大幅提高。扎来普隆自乳化制剂家兔体内的生物利用度提高了3.5倍。
另一种热熔造粒则是将难溶性主药与硅酸铝镁(NEUSILIN®)直接热熔造粒,如将舒林酸与硅酸铝美共同熔融造粒,并与球磨混合物以及原晶体的溶出进行了研究,得到了几条有意思的溶出曲线,见图24所示。

图24舒林酸制剂溶出曲线比较
从图可见,原晶体药物溶出最差,当舒林酸与硅酸铝镁(NEUSILIN®)按1:1比例制成共融颗粒后,溶出量与二者1:1的球磨物相当;当将舒林酸与硅酸铝镁(NEUSILIN®)比例变成1:2制成共熔物时,舒林酸的溶出速度迅速提高,显然这一比例更适合于制备成舒林酸的速释制剂。而前者或者球磨物是否具有制备缓释制剂的可能呢。图25为在40℃RH75%环境下不同时间存放的球磨物和热熔造粒样品X-射线衍射数据对比分析,所有样品在加速状态下存放3-4个月,仍保持无定型状态。
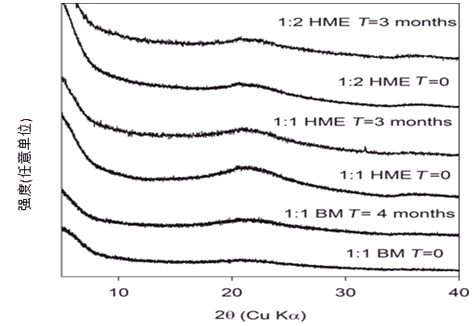
图25.舒林酸不同样品X-射线衍射图谱
(五)固体脂质纳米粒子技术(SLN)
固体脂质纳米粒子技术是基于固体脂质的新型药物输送系统的通用乳剂。粒径分布大约在10-1000nm之间。图26是固体脂质纳米粒子和纳米乳的区别示意图。制备固体脂质纳米粒子存在一些瓶颈问题,但是通过利用硅酸铝镁(NEUSILIN®)的优良性能,可以克服这些瓶颈问题,见图27所示。

图26.固体脂质纳米粒子和纳米乳示意图
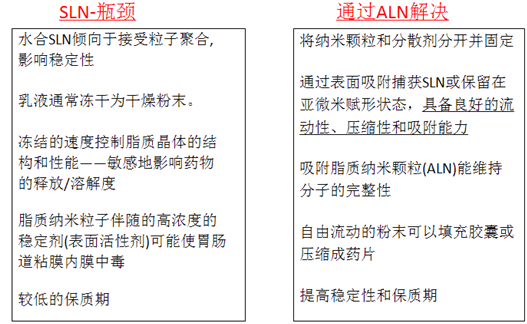
图27.固体脂质纳米粒子制备瓶颈及对策
固体脂质纳米粒子制备过程示意图见图28所示。图29是卡维地洛固体脂质纳米粒子的制备工艺。
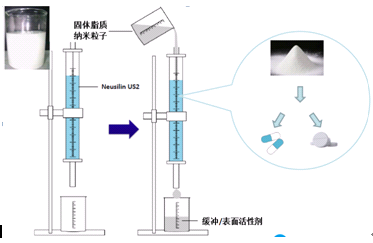
图28. 固体脂质纳米粒子制备过程示意图

图29.卡维地洛脂质纳米粒子制剂的制备过程
称取卡维地洛+硬脂酸,用二氯甲烷:甲醇(2:1)溶解,将此溶液滴加至牛磺胆酸钠缓冲液中超声乳化,加1%聚乙烯醇后,冷冻,形成纳米脂质粒子,加入硅酸铝镁(NEUSILIN®US2)吸附,干燥,压片或装胶囊。
表8.磷酸卡维地洛脂质纳米吸附颗粒
吸附效率(%):7-8ml吸附脂质纳米颗粒/50mgUS2
卡维地洛吸附脂质纳米颗粒的药物溶出及稳定性考察结果见图30所示。
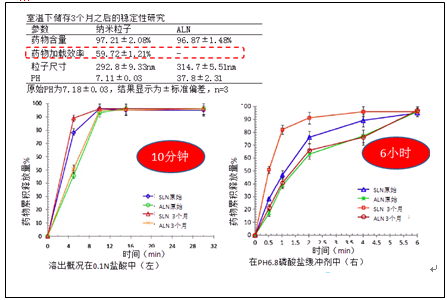
图30.卡维地洛固体脂质纳米粒子颗粒的溶出及稳定性考察结果
五.硅酸铝镁(NEUSILIN®)在药剂学中的研究与应用之展望
近年来,国外对硅酸铝镁(NEUSILIN®)在药剂学中的研究与应用已经非常广泛,表9为近期在药物制剂处方中使用了硅酸铝镁的药物类型;表10为不同药物制剂所用硅酸铝镁(NEUSILIN®)的型号以及在处方中所起的作用;表11为两种型号的硅酸镁铝((NEUSILIN®)US2和UFL2)在不同药物制剂处方中的应用及所起的作用。
表9.近期将硅酸铝镁(NEUSILIN®)用于制剂处方的药物
表10.不同药物制剂所用硅酸铝镁(NEUSILIN®)的型号以及在处方中所起的作用
表11.不同药物制剂所用硅酸铝镁(NEUSILIN®)的型号以及在处方中所起的作用
对药剂学工作者来说,硅酸铝镁(NEUSILIN®)确实是一种处方设计不可多得的辅料,相信,随着药剂学科研究的深入发展,我们对这一辅料的认识必将更加深刻。关于硅酸铝镁(NEUSILIN®)的国内注册信息,国内尚无企业研发及生产同类产品。日本富士化学株式会社已经于2012年提出在我国的进口注册申请,目前仍处于审评阶段。据悉日本富士化学株式会社已与北京森昌泰和科技有限公司签订了全国代理销售协议,有兴趣者可向该公司咨询并获取研究用样品。据笔者所知,我国药剂学领域对硅酸铝镁(NEUSILIN®)的认识、研究以及应用仍处于初级水平,作为一名药剂学工作者,有必要将硅酸铝镁(NEUSILIN®)的系统知识和近年来在制剂领域研究与应用的进展介绍给大家,故整理了本综述,以期为国内广大的药剂学工作者在制剂的处方设计和研究工作中增加一种新的选择。因本人水平有限,难免有谬误之处,需要时还请各位对硅酸铝镁(NEUSILIN®)有兴趣者阅读原文献,本综述仅供参考。
六.部分参考文献
1.Suhas G.et al:Journal of the American Association of Pharm. Sci,30:1114,2013
2.Mladen M.et al: Inter. Journal. of Pharmaceutics,436(1-2):58-65;06/2012
3.Deepak B.et al:Pharm.Dev.and Technolog, 13:255–269, 2008
4.Manish K.et al: Pharm. Dev. and Technology, 6(4), 563–572 (2001)
5. C.M. Hentzschel et al:Eur.Journal.of Pharm.and Biopharm.80130-135 (2012)
6. Karthik Y. Janga et al:Journal of Microencapsulation, 2013; 30(2): 161–172
7.Jenifer M et al: Journal of pharm.and biopharm.sci,Vol100,No.8 August,2011
8.Paola Mura,et al: Pharm. Devel. and Technology, 2012; 17(3): 277–284
9. Venkata Raman Kallakunta, et al:Powder Technology,221,375-382(2012)
10. R. Neslihan Gursoy et al: Biomedicine & Pharmacotherapy 58 (2004) 173–182
11. Camilla S. et al:AAPS PharmSciTech, Vol. 10, No. 4, December 2009 (# 2009)
12. Ambarish H. Vadher, et al: AAPS PharmSciTech, Vol. 10, No. 2, June 2009 (# 2009)
13.Anna K. et al:Thermochimica Acta,509,12-17(2012)
一个喜欢酒后吹牛的药剂学工作者的综述
吹牛(二)
硅酸铝镁(NEUSILIN®)是一种非晶态无定型粉末,包含铝的四面体或八面体,镁的八面体和硅的四面体,几者随机连接形成一个复杂的三维结构,而不是由单一明确的单体结构重复排列而成。自上世纪60年代由日本富士化学公司将硅酸铝镁开发作为药用辅料上市至今,已有近60年的历史。由于其特殊的分子结构及立体构型,使其具有良好的流动性、可压性、吸附性、粘合性、粉体性、填充性以及助悬性等特点,从而使其在药物制剂的应用领域发挥了卓越的作用。随着现代药剂学的研究进展,近期,又不断发现了一些硅酸镁铝在制剂设计方面的新用途,为其展示出更为广阔的应用前景。
一.化学结构与一般性质
化学结构式及电镜照片如图1所示:

图1.化学结构式及电镜照片
CAS号:1327-43-1
性状:白色,无嗅粉末。几乎不溶于水和乙醇,可溶于热的稀盐酸。
pH值:(4%水浆)6.0-8.0。
干燥失重:小于20%。
酸消耗量:按干燥品计算,每克硅酸铝镁消耗0.1mol/L的盐酸不低于210ml。
二.安全性
急性毒性:按照600-6000mg/kg的剂量标准给雌性小鼠灌胃,连续14天。在6000mg/kg剂量组中,观察到小鼠体重呈下降趋势,自发运动减少,但是,停止灌胃后第10天,上述症状得到恢复。
亚急性毒性:Ueno等人与1978年做了一项关于硅酸铝镁的毒性实验,按照1500mg/kg剂量与甘草提取物一起给Wister immichi大鼠灌胃,连续给药30天,没有显示任何毒性反应。在体重、食物与水的消耗量、血液学、生化以及鸟检测,对照组与实验组没有显著性差别。尸检和组织学检查也未见明显病变,证明了硅酸铝镁的安全性良好。
最大用量:硅酸铝镁(NEUSILIN®)是一种安全性较高的辅料,根据日本医药添加剂百科全书(Encyclopedia of the pharmaceutical additives, Japan, 2005)规定,每日口服最大用量为1.05g。
三. 硅酸铝镁(NEUSILIN®)的型号与特性
硅酸铝镁(NEUSILIN®)共有11种型号,表1列出了4种常用型号的物理性能,见表1所示。型号的区分取决于pH值(水浆液)、粉末或颗粒以及水分含量等。表2介绍了两种型号硅酸铝镁对难闻性气味的吸附能力。
表1.硅酸铝镁的型号与各项性能指标对比
| 型号 | S1 | FH2 | US2 | UFL2 |
| 5%混浆pH值 | 9.4 | 9.7 | 7.4 | 7.4 |
| 外观 | 颗粒 | 粉末 | 颗粒 | 粉末 |
| 吸油量(ml/g) | 1.3 | 1.5 | 3.2 | 3.2 |
| 粒径分布(μm) | 70-110 | 10-20* | 60-120 | 2-8* |
| 未通过330目筛余留(%) | <10 | <0.5 | ||
| 比表面积(m2/g) | 110 | 110 | 300 | 300 |
| 休止角 | 30 | 45 | 30 | 45 |
| 松密度(g/ml) | 0.33 | 0.31 | 0.15 | 0.08 |
| 实密度(g/ml) | 0.40 | 0.43 | 0.19 | 0.13 |
| 干燥失重(%) | 16 | 2.8 | 1.4 | 1.8 |
表2.硅酸铝镁((NEUSILIN®NFL2)对难闻性气味的吸附能力
| 难闻气体 | 浓度/用量 | 气味消除率(%) |
| 氨水 | 1000ppm/100mg | 79.5 |
| 氨水 | 1000ppm/200mg | 96.2 |
| 三乙胺 | 435ppm/100mg | 81.6 |
| 硫化氢 | 697ppm/100mg | 31.4 |
| 异戊酸 | 262ppm/20mg | 100 |
| 醋酸 | 849.8ppm/100mg | 99.6 |
| 丙酸 | 382.3ppm/20mg | 100 |
| 正丁酸 | 311.8ppm/20mg | 100 |
四.硅酸铝镁在药剂学中的应用
从生物药剂学的观点出发,通常认为药物从固体剂型中的溶出依赖于溶解性,药物的吸收则依赖于渗透性。固体剂型的设计能否达到的生物药剂学及物理药剂学要求,取决于所用辅料及其制剂工艺。硅酸铝镁的物理特性赋予其在药物制剂处方设计的独特功能,试归纳其特点如下:
1. 直接可压和助压缩性,提高片剂的硬度、粉体的流动性、防静电以及防止粉体结块。
2. 具有高容量油脂吸附作用,使油状药物固体化。
3. 可提高易潮解药物吸湿稳定性。
4. 便于亲水性低熔点原料药物的压片。
5. 提高制剂处方的稳定性。
6. 缓控释处方的组成。
7. 通过球磨或固体分散技术,提高生物利用度等。
8. 提高固体制剂的外观质量。
表3.不同型号硅酸铝镁(NEUSILIN®)的用途应用和用量
| 类别 | S1 | FH2 | US2 | UFL2 |
| 片剂的粘合剂、崩解剂、提高硬度 | 5-20% | 5-20% | 1-10% | 1-10% |
| 吸附剂 | 5-20% | - | 2-10% | 2-10% |
| 增加流动性 | - | - | - | 0.5-5% |
| 提高易潮解药物的稳定性 | - | - | 5-15% | 5-15% |
| 赋形剂或稀释剂 | - | - | 30-90% | 30-90% |
| 液体药物固体化 | - | - | - | 30-50% |
| 固体分散 | 20-50% | 20-50% |
表3为不同型号硅酸铝镁(NEUSILIN®)作为制剂添加剂不同用途及常规用量。前面介绍了硅酸铝镁的一般性能,以下从五个方面介绍硅酸铝镁在药剂学中研究与应用的案例及部分研究结果。
(一)提高片剂的硬度、粉体的流动性、防静电以及防止粉体结块等
图2是不同硅酸盐对淀粉-乳糖片硬度的影响,由图可见,处方中添加10%的硅酸铝镁(NEUSILIN®US2)与10%硅酸钙片剂的硬度相当,而添加硅胶处方的片剂硬度最低。硅酸铝镁(NEUSILIN®)单独与乳糖配伍压片,其增加片剂硬度的作用也是显而易见的,见图3所示。

图2.玉米淀粉-乳糖-硅酸盐组方对片剂硬度的影响

图3.硅酸铝镁(NEUSILIN®)对乳糖压片硬度的影响
图4为在马铃薯淀粉中加入不同浓度的硅酸盐后,粉体的休止角变化曲线。

图4.在马铃薯淀粉中加入硅酸盐的休止角曲线
图4为在马铃薯淀粉中加入不同浓度的硅酸盐后,粉体的休止角变化曲线。硅酸铝镁(NEUSILIN®)降低马铃薯淀粉的休止角用量最低。图5为硅酸铝镁(NEUSILIN®)与马铃薯淀粉混合后的电镜照片,硅酸铝镁(NEUSILIN®)是均匀粘附的于马铃薯淀粉颗粒的表面,就是这样起到增加流动性、防结块以及防静电作用的。

图5.硅酸铝镁与马铃薯淀粉混合后的电镜照片
在高湿条件下防止药物结块的典型例子是天冬氨酸钠,如图6所示。在天冬氨酸钠中加入5%的硅酸铝镁(NEUSILIN®),置RH75%环境下露置2天,仍能保持为松散的颗粒状,而不加硅酸铝镁(NEUSILIN®)者则明显结成了块状。

图6.硅酸铝镁的防天冬氨酸钠吸潮结块作用
表4是一组扑热息痛片剂处方,其中处方2、3、5含有2%的硅酸铝镁(NEUSILIN®UFL2),将试制的片剂于40℃,RH75%条件下放置1个月,所有加入硅酸铝镁(NEUSILIN®)片剂的硬度均无明显变化,而未加硅酸铝镁(NEUSILIN®)片的硬度则明显降低,溶出度未见明显变化,见图7所示。
表4.提高片剂硬度和溶出稳定性
| 组成(mg) | 编号 | ||||
| 处方1 | 处方2 | 处方3 | 处方4 | 处方5 | |
| 扑热息痛 | 15 | 15 | 15 | 15 | 15 |
| 乳糖 | 103.5 | 100.5 | 93 | - | - |
| 甘露醇 | - | - | - | 96 | 93 |
| 微晶纤维素 | 30 | 30 | 30 | 30 | 30 |
| UFL2 | - | 3 | 3 | - | 3 |
| L-HPC | - | - | 7.5 | 7.5 | 7.5 |
| 硬脂酸镁 | 1.5 | 1.5 | 1.5 | 1.5 | 1.5 |
| 总量 | 150 | 150 | 150 | 150 | 150 |

图7.硅酸铝镁(NEUSILIN®)对扑热息痛片硬度和溶出的影响
(二)油状药物的固体化或粉末化
有些药物属于油状液体,除了可以制成软胶囊外,有时也需要制成其他固体制剂或固体制剂添加剂,如脂溶性维生素类、DHA、挥发油等,有些难溶性药物还可用油脂类物质溶解,进而制成固体制剂,这都需要采用油状物质的固体化技术。硅酸铝镁(NEUSILIN®)的出现,为此类制剂的处方设计提供了有效的手段。从表1和图8可知,两种硅酸铝镁(Neusilin®US2和Neusilin®UFL2)的吸油能力达到3g/ml以上,可见其吸油能力之卓越。表5列出了以硅酸铝镁为吸附剂的亚麻油片的三种处方,由表5可见,添加有硅酸铝镁(Neusilin®US2)的处方,片剂硬度明显高于添加气相二氧化硅的处方。由图9可见,以硅酸铝镁(NEUSILIN®)为吸附剂,获得的亚麻油粉末经50℃干燥后,外观良好,明显优于气相二氧化硅和微粉硅胶作为吸附剂制成的产物外观。
表5.硅酸铝镁(NEUSILIN®)对亚麻油吸附片硬度的影响
| 组分(g) | 处方1 | 处方2 | 处方3 |
| 亚麻油 | 30 | 40 | 30 |
| US2 | 66 | 56 | - |
| 气相二氧化硅 | 66 | ||
| 交联羧甲基纤维素 | 3 | 3 | 3 |
| 硬脂酸镁 | 1 | 1 | 1 |
| 500kg/m2压片的片剂硬度 | 153N | 120N | 50-60N |
| 1000 kg/m2压片的片剂硬度 | 270N | 140N |

图8.不同硅酸盐吸附亚麻油的能力

图9.不同硅酸盐吸附亚麻油粉末化产物外观(50℃干燥后)
图10为维生素E与微晶纤维素混合压片张力强度与压缩压力的关系(左),图以及为维生素E与硅酸铝镁(NEUSILIN®)混和压片张力强度与压缩压力的关系(右)。

图10.维生素E与不同吸附剂混合压片后张力强度与压缩压力的关系
图11维生素E与微晶纤维素混合压片崩解时间与张力强度的关系(左),以及为维生素E与硅酸铝镁(NEUSILIN®)混和压片崩解时间与张力强度的关系(右)。

图11.维生素E与不同吸附剂混合后压片崩解时间与张力强度的关系
图12为维生素E片的溶出曲线,维生素E的溶出效果以硅酸铝镁(NEUSILIN®)为吸附剂压出的片剂优于以气相硅胶为吸附剂的片剂。图13是DHA片的处方以及两种处方片剂强度和溶出与压缩压力的关系。

图12.维生素E片在pH1.2人工胃液中的溶出曲线

图13.硅酸铝镁(NEUSILIN®)吸附的鱼油片强度与压缩压力的关系
(三)固体药物通过与硅酸铝镁共研磨达到药物晶体的无定型化
选择合适的辅料与晶型难溶性药物药物进行研磨,可以药物晶形转变为无定型,并可防止再结晶、可提高润湿性、溶解度、溶出度乃至提高主药的生物利用度,硅酸铝镁(NEUSILIN®)就是这种研磨辅料的首选。因为硅酸铝镁含有多个硅醇基,通过与晶型药物共同研磨(或球磨),可与药物形成氢键结合,从而改善药物的物理性能。但这类研磨物不适合那些因晶型改变而稳定性下降的药物。对热敏感性药物可以考虑采用冷冻研磨方式。

图14.研磨物制备示意图
Gupta等的研究报告表明,通过球磨的硅酸铝镁(NEUSILIN®)与一些药物如酮洛芬、吲哚美辛、萘普生和黄体酮等,可显著改善这些难溶性药物制剂的溶出度。其中与酮洛芬、吲哚美辛和萘普生在研磨过程中,酸性药物与硅酸铝镁产生酸碱反应,使主药形成无定型粉末,而黄体酮则是与中性硅酸铝产生了氢键结合,进而使主药形成无定型粉末。上述无定形粉末的X-射线衍射图谱中,主药晶体的衍射峰明显消失,经过加速试验稳定性考察(4周)证明,物理稳定性仍然良好。
醋氯芬酸与硅酸铝镁研磨物使醋氯芬酸的溶解性大幅提高。布洛芬与硅酸铝镁(NEUSILIN®)可形成溶解性更高的盐。

图15.吲哚美辛与US2研磨混合物的X-射线衍射图谱
(四)固体分散技术
此类制剂设计的主要目的是提高难溶性药物的溶出速度及生物利用度。图16是固体分散制剂组成示意图。

图16.无定形固体分散制剂组成示意图
不同的难溶性药物需要采用不同的固体分散物制备方法。图17是三种药物的固体分散体制备方法。图中标示的载体是指吸附剂,具有强大吸附能力的硅酸铝镁也许是最佳选择。图中的SMEDDS/SEDDS的含义是自乳化释药系统。
(1)熔融法:药物+聚合物以及表面活性剂共融,加载体(或不加)制成其他剂型。
(2)溶剂法:药物溶解+载体,加聚合物或与表面活性剂的混合物,脱除溶剂(或不脱),制成其他制剂。
(3)乳化法:药物溶于油,加表面活性剂或辅助表面活性剂,加载体,制成自乳化系统,进一步制成其他制剂。
上述三种固体分散技术均可使用硅酸铝镁(NEUSILIN®)作为载体。其次,关于表面活性剂的使用也不是绝对的,仅仅是在处方设计没有达到预期时才使用。用硅酸铝镁(NEUSILIN®)作为固体分散物载体具有载药量大、流动性好、可压性强、比表面积大、吸附能力好以及保护药物免受湿气影响的能力强等特点。

图17.三种固体分散物制备方式
图18是Gupta等发表的7种难溶性药物的固体分散物制备方法。图19和图20是难溶性丁酸类药物BAY-12-9556固体分散物和物理混合物的溶出曲线。

图18.七种难溶性药物的固体分散物制备方法

图19.难溶性药物BAY-12-9556固体分散物和物理混合物的溶出曲线

图20.不同配方的溶出曲线
图20中各条曲线的样品中主药成分BAY-12-9556与硅酸铝镁比例均为1:1,但硬脂酸聚乙二醇甘油酯的比例分别为0.5、1和1.5,随着硬脂酸聚乙二醇甘油酯比例的升高,溶出速度明显提高。
将难溶性药物二氢吡啶类药物用脂肪酸甘油酯类物质溶解,然后用硅酸铝镁(NEUSILIN®)吸附,再进一步制成固体制剂,也可获得较高的生物利用度的制剂。处方1和处方3的生物利用度分别为23%和29.4%,对照药(不加添加剂)仅为0.3%,而且在60℃连续加热4周,有关物质未见明显增加,稳定性良好。
表6.二氢吡啶衍生物的处方设计
| 组分 | 处方1 | 处方2 | 处方3 |
| 用量(g) | |||
| 二氢吡啶衍生物 | 20.1 | 20.1 | 20.1 |
| 不饱和脂肪酸甘油酯 | 650 | - | 325 |
| 聚氧乙烯单油酸酯 | - | 650 | 325 |
| US2 | 370 | 370 | 370 |
| CMC-Na | 30 | 30 | 30 |
| 纯化水 | 250 | 250 | 250 |
2008年,Catarzi等发表了格列本脲自乳化固体分散释药系统的研究报告,他们选择了三种硅酸盐作为吸附剂,处方设计见表7。该报告还强调不能使用Aersil380、R972、200和Zeopharm177等作为吸附载体,因为会导致自乳化吸附后,流动性降低。图21为格列本脲自乳化制剂的的溶出曲线。
表7.格列本脲自乳化固体分散释药系统处方
| 吸附剂 | 硅酸铝镁(NEUSILIN®) | Aeroperl® | Zeopharm® |
| 格列本脲(g) | 5 | 5 | 5 |
| 自微乳配方(ml)* | 800 | 800 | 800 |
| 吸附剂(mg) | 350 | 350 | 350 |
| CMC-Na(mg) | - | 400 | 400 |
| 交联CMC-Na(mg) | 95 | 50 | 50 |
| 硬脂酸镁(mg) | 5 | 10 | 10 |
| 片重(mg) | 1255 | 1615 | 1615 |
| 硬度(N) | 50 | 30 | 10 |
| 崩解时间(min) | 9-12 | 8-13 | - |
*800ml自乳化配方:聚氧乙烯甘油癸酸酯(Labrafac-Hydro®)作为油相,吐温20作为表面活性剂,二乙二醇单乙基醚作为辅助表面活性剂。

图21.格列本脲SMEDDS溶出曲线
Agarwal等人2009年用不同型号的硅酸铝镁Neusilin®和其他一些硅酸盐与灰黄霉素制备成自乳化释药系统,其中硅酸铝镁Neusilin® UFL2D自乳化制剂显示最高的溶出度(1小时>90%),并观察到其具有最大的吸附率,达到2.75ml/g,说明这种自乳化制剂的溶出度与吸附剂粒子的大小及其比表面积有明显的相关性。图22为这一系统的配方和制备过程及混合粉末的流变学数据。图23为采用不同载体作为吸附剂的溶出曲线,并与原料药粉末作对比。

图22.灰黄霉素自乳化制剂配方、制备过程及混合粉末的流变学数据


图23.灰黄霉素自乳化释药系统的溶出曲线
Suhas G. Gumaste等报道了不同硅酸盐吸附油脂和表面活性剂对压片性质和表面结构的影响,结果表明:6种硅酸盐按1:1比例吸附Capmul®MCM EP(甘油癸酸酯)、Captex®355 EP/ NF(辛酸/癸酸甘油三酯)和Cremophor®EL(PEG-35蓖麻油)后,加入20%的微晶纤维素后压片,测量片剂的抗张强度。硅酸铝镁Neusilin®®US2是唯一能够生产出具有可接受的抗张强度的片剂,表面结构研究发现脂质液体是被吸附到的硅酸盐孔隙中。
Mladen等报道了水难溶性药物卡马西平固体自微乳化药物递送系统(SSMEDDS),处方中选用的表面活性剂为吐温80和辅助表面活性剂PEG-40氢化蓖麻油和油辛酸/癸甘油三酯,表面活性剂与辅助表面活性剂的比率为1:1,分别采用4种硅酸盐作为吸附剂,为Neusilin®(®)UFL2、Neusilin®(®)FL2、SYLYSIA(®)320和SYLYSIA(®)350。研究发现(SSMEDDS)制剂可改变卡马西平的溶出速率,吸附剂的类型对卡马西平的溶出速率也有显著影响。
另有文献报道了采用硅酸铝镁(NEUSILIN®)为吸附剂,将扎来普隆、优降糖、盐酸乐卡地平、环抱素A以及帕潘立酮等难溶性药物制成纳米自乳化粉末或片剂,均使主药的溶解性和溶出度大幅提高。扎来普隆自乳化制剂家兔体内的生物利用度提高了3.5倍。
另一种热熔造粒则是将难溶性主药与硅酸铝镁(NEUSILIN®)直接热熔造粒,如将舒林酸与硅酸铝美共同熔融造粒,并与球磨混合物以及原晶体的溶出进行了研究,得到了几条有意思的溶出曲线,见图24所示。

图24舒林酸制剂溶出曲线比较
从图可见,原晶体药物溶出最差,当舒林酸与硅酸铝镁(NEUSILIN®)按1:1比例制成共融颗粒后,溶出量与二者1:1的球磨物相当;当将舒林酸与硅酸铝镁(NEUSILIN®)比例变成1:2制成共熔物时,舒林酸的溶出速度迅速提高,显然这一比例更适合于制备成舒林酸的速释制剂。而前者或者球磨物是否具有制备缓释制剂的可能呢。图25为在40℃RH75%环境下不同时间存放的球磨物和热熔造粒样品X-射线衍射数据对比分析,所有样品在加速状态下存放3-4个月,仍保持无定型状态。

图25.舒林酸不同样品X-射线衍射图谱
(五)固体脂质纳米粒子技术(SLN)
固体脂质纳米粒子技术是基于固体脂质的新型药物输送系统的通用乳剂。粒径分布大约在10-1000nm之间。图26是固体脂质纳米粒子和纳米乳的区别示意图。制备固体脂质纳米粒子存在一些瓶颈问题,但是通过利用硅酸铝镁(NEUSILIN®)的优良性能,可以克服这些瓶颈问题,见图27所示。

图26.固体脂质纳米粒子和纳米乳示意图

图27.固体脂质纳米粒子制备瓶颈及对策
固体脂质纳米粒子制备过程示意图见图28所示。图29是卡维地洛固体脂质纳米粒子的制备工艺。

图28. 固体脂质纳米粒子制备过程示意图

图29.卡维地洛脂质纳米粒子制剂的制备过程
称取卡维地洛+硬脂酸,用二氯甲烷:甲醇(2:1)溶解,将此溶液滴加至牛磺胆酸钠缓冲液中超声乳化,加1%聚乙烯醇后,冷冻,形成纳米脂质粒子,加入硅酸铝镁(NEUSILIN®US2)吸附,干燥,压片或装胶囊。
表8.磷酸卡维地洛脂质纳米吸附颗粒
| 参数 | 结果 |
| 吸附效率(%) | 71.8+-1.42 |
| 粒径nm | 309.4+-7.5 |
| 分散指数 | 0.164+-0.08 |
| 休止角 | 37.8+-2.31 |
卡维地洛吸附脂质纳米颗粒的药物溶出及稳定性考察结果见图30所示。

图30.卡维地洛固体脂质纳米粒子颗粒的溶出及稳定性考察结果
|
|
五.硅酸铝镁(NEUSILIN®)在药剂学中的研究与应用之展望
近年来,国外对硅酸铝镁(NEUSILIN®)在药剂学中的研究与应用已经非常广泛,表9为近期在药物制剂处方中使用了硅酸铝镁的药物类型;表10为不同药物制剂所用硅酸铝镁(NEUSILIN®)的型号以及在处方中所起的作用;表11为两种型号的硅酸镁铝((NEUSILIN®)US2和UFL2)在不同药物制剂处方中的应用及所起的作用。
表9.近期将硅酸铝镁(NEUSILIN®)用于制剂处方的药物
| 镇痛类非甾体抗炎剂 | 抗生素 | 油状活性物质 |
| 巴拉本非 | 克拉霉素 | 维生素E醋酸酯 |
| 奥沙普秦 | 氯霉素 | 普劳诺托 |
| 水杨酸甲酯 | 磷霉素 | |
| 洛索洛芬 | 罗红霉素 | |
| 氟芬那酸 | 舒他西林 | |
| 奥磺酸钠 | 头孢氨苄 | |
| 吸湿性药物 | 水难溶性原料药 | 酶制剂 |
| L-天冬氨酸钾 | 阿昔洛韦 | 舍雷肽酶 |
| 普伐他丁钠 | 酒石酸艾芬地尔 | 高氏淀粉酶 |
| 丙戊酸钠 | 盐酸西曲酸酯 | 蛋白酶 |
| 巯甲基蛋氨酸 | 盐酸地芬尼多 | 复合淀粉酶 |
| 阿替洛尔 | 溶菌酶 | |
| 氯地孕酮醋酸酯 | 混合酶 |
表10.不同药物制剂所用硅酸铝镁(NEUSILIN®)的型号以及在处方中所起的作用
| 活性成分 | 硅酸铝镁型号 | 添加剂作用 |
| 盐酸左旋肉碱 | UFL2-fujicalin(2:1) | 保湿,增加流动性 |
| 改善血液循环草药 | US2 | 软胶囊改成片剂 |
| 草酸萘呋胺 | UFL2 | 增加流动性 |
| 沙坦类降压药 | UFL2 | |
| 红三叶异黄酮 | US2 | |
| 奥美沙坦 | US2 | 以溶剂吸附形式与原料药作用 |
| 非洛地平 | US2+UFL2 | 以油/表面活性剂吸附形式与原料药作用 |
| 二甲双胍 | UFL2 | 提高流动性 |
| 替米沙坦 | US2 | 以溶剂吸附形式与原料药作用 |
| 西甲硅油 | US2 | 油状药物的固体化、粉末化 |
| 油状脂溶性维生素 | US2、UFL2 | 油状药物的固体化、粉末化 |
表11.不同药物制剂所用硅酸铝镁(NEUSILIN®)的型号以及在处方中所起的作用
| 硅酸铝镁 | 项目 | 用途 |
| (NEUSILIN®)UFL2 | 中药提取物 | 抗结块和改善流动性 |
| 复合维生素 | 吸附剂和改善流动性 | |
| 卵磷脂 | 防止结块和加速崩解 | |
| 阿伐他汀钙 | 提高硬度和改善脆性 | |
| 乙胺丁醇+异烟肼 | 防止结块 | |
| 阿卡波糖 | 吸附剂和改善流动性 | |
| 辅酶Q10 | 防止结块 | |
| 叶黄素+胡萝卜素 | 防止结块 | |
| 拉维酸 | 防止结块和提高稳定性 | |
| 布洛芬 | 防止结块 | |
| 来曲唑 | 改善流动性,稀释剂 | |
| 尼莫地平 | 改善溶出,提高生物利用度 | |
| (NEUSILIN®)US2 | ALA(蚕丝肽) | 防止结块和加速崩解 |
| 左旋肉碱 | 防止结块和加速崩解 | |
| 油溶性维生素 | 吸附剂,液体固体化颗粒 | |
| 流浸膏 | 吸附剂,液体固体化颗粒 |
对药剂学工作者来说,硅酸铝镁(NEUSILIN®)确实是一种处方设计不可多得的辅料,相信,随着药剂学科研究的深入发展,我们对这一辅料的认识必将更加深刻。关于硅酸铝镁(NEUSILIN®)的国内注册信息,国内尚无企业研发及生产同类产品。日本富士化学株式会社已经于2012年提出在我国的进口注册申请,目前仍处于审评阶段。据悉日本富士化学株式会社已与北京森昌泰和科技有限公司签订了全国代理销售协议,有兴趣者可向该公司咨询并获取研究用样品。据笔者所知,我国药剂学领域对硅酸铝镁(NEUSILIN®)的认识、研究以及应用仍处于初级水平,作为一名药剂学工作者,有必要将硅酸铝镁(NEUSILIN®)的系统知识和近年来在制剂领域研究与应用的进展介绍给大家,故整理了本综述,以期为国内广大的药剂学工作者在制剂的处方设计和研究工作中增加一种新的选择。因本人水平有限,难免有谬误之处,需要时还请各位对硅酸铝镁(NEUSILIN®)有兴趣者阅读原文献,本综述仅供参考。
六.部分参考文献
1.Suhas G.et al:Journal of the American Association of Pharm. Sci,30:1114,2013
2.Mladen M.et al: Inter. Journal. of Pharmaceutics,436(1-2):58-65;06/2012
3.Deepak B.et al:Pharm.Dev.and Technolog, 13:255–269, 2008
4.Manish K.et al: Pharm. Dev. and Technology, 6(4), 563–572 (2001)
5. C.M. Hentzschel et al:Eur.Journal.of Pharm.and Biopharm.80130-135 (2012)
6. Karthik Y. Janga et al:Journal of Microencapsulation, 2013; 30(2): 161–172
7.Jenifer M et al: Journal of pharm.and biopharm.sci,Vol100,No.8 August,2011
8.Paola Mura,et al: Pharm. Devel. and Technology, 2012; 17(3): 277–284
9. Venkata Raman Kallakunta, et al:Powder Technology,221,375-382(2012)
10. R. Neslihan Gursoy et al: Biomedicine & Pharmacotherapy 58 (2004) 173–182
11. Camilla S. et al:AAPS PharmSciTech, Vol. 10, No. 4, December 2009 (# 2009)
12. Ambarish H. Vadher, et al: AAPS PharmSciTech, Vol. 10, No. 2, June 2009 (# 2009)
13.Anna K. et al:Thermochimica Acta,509,12-17(2012)
上一篇:没有了
下一篇:聚乙烯蜡微粉在油漆和油墨中的应用
Copyright 2006-2018 北京森昌泰和科技有限责任公司,All Rights Reserved. 京ICP备11033684号

